а) Паління тютюну:ризик розвитку раку гортані більше у людей, які в даний час палять, або коли-небудь палили в минулому, ніж у тих, хто ніколи не палив. Ризик зростає зі збільшенням тривалості і частоти куріння сигарет.
б) Історія паління
Для оцінки паління як фактору ризику використовується індекс курця (ІК), який вимірюється у пачко/роках:
ІК (пачко/роки) - (кількість цигарок на добу x стаж паління (роки)
Група високого ризику виникнення раку гортані:
або
Група середнього ризику виникнення раку гортані:
Група низького ризику виникнення раку гортані:
в) Вплив радону у приміщеннях.
г) Вплив професійних канцерогенних факторів (миш'як, хром, азбест, нікель, кадмій, берилій, кремній, дизельне паливо)
д) Онкологічний сімейний анамнез.
е) Пасивне паління.
є) Історія захворювань (хронічні захворювання гортані в анамнезі).
Класифікація раку гортані за системою TNM сьомого перегляду (2009)
T – клінічна класифікація
Т – первинна пухлина
TX – недостатньо даних для первинної пухлини.
T0 – первинна пухлина не визначається.
Tis – преінвазивна карцинома (carcinoma in situ).
Т1 – пухлина обмежена одною анатомічною частиною надголосникової області рухомість голосових зв’язок збережена.
Т2 – пухлина вражає слизову оболонку декількох анатомічних частин надголосникової області чи одну частину надгоолосникової області і одну або декілька частин голосових зв'язок (наприклад, медіальної стінки грушовидного сінуса), рухомість голосовых зв’язок збережена.
Т3 – пухлина обмежена гортанню з фіксацією голосових зв'язок і/або з розповсюдженням на позаперстневидну область чи переднадгортанні тканини.
Т4а – пухлина поширюється на щитовидний хрящ і/чи інші тканини біля гортані: трахею, щитовидну залозу, стравохід, м’які тканини шиї, включно з глибокими м’язами язика (підборідно-язиковий, под’язично-язиковий, піднебінно-язиковий і шиловидно-язиковий), підпід’язичні м’язи.
Т4b – пухлина поширюється на превертебральний простір, медіастінальні структури або охоплює сонну артерію.
Т1 – пухлина обмежена голосовою(ими) зв’язкою(ами) без порушення рухомості (можуть бути залучені передня чи задня комісури).
Т1а – пухлина обмежена одною голосовою зв’язкою.
Т1b – пухлина розповсюджується на обидві голосові зв’язки.
Т2 – пухлина розповсюджується на надголосникову і/чи підголосникову області, і/або порушення рухомості голосової зв’язки, і/або розповсюджується за межі голосової щілини, і/чи з невеликою ерозією щитовидного хряща (наприклад: внутрішній кортикальний шар).
Т3 –на обмежена гортанню із фіксацією голосової зв’язки.
Т4а – пухлина розповсюджується на щитовидний хрящ і/чи на інші тканини біля гортані: трахею, щитовидну залозу, стравохід, м’які тканини шиї, із залученням глибоких м’язів язика (язика (підборідно-язиковий, под’язичково-язичковий, піднебінно-язичковий і шиловидно-язиковий), підпід’язичні м’язи.)
Т4b – пухлина поширюється на превертебральний простір, медіастінальні структури або охоплює сонну артерію.
Т1 – пухлин а обмежена підголосниковою областю.
Т2 – пухлина поширюється на одну або обидві голосові зв’язки з вільною або обмеженою рухомістю.
Т3 – пухлина обмежена гортанню з фіксацією голосової зв’язки.
Т4а – пухлина розповсюджується на щитовидний хрящ і/чи на інші тканини біля гортані: трахею, щитовидну залозу, стравохід, м’ягкі тканини шиї, із залученням глибоких м’язів язика (язика (підборідно-язиковий, під’язиково-язиковий, піднебінно-язиковий і шиловидно-язиковий), підпід’язичні м’язи
Т4b – пухлина поширюєтьсятся на превертебральний простір, медіастінальні структури або окутує сонну артерію.
NХ - недостатотрньо данних для оцінки стану регіонарних лімфатичних вузлів.
N0 – немає ознак метастатичногоого враження регіонарних лімфатичних вузлів.
N1 – метастази в одному лімфатичному вузлі на стороні ураження до 3 см і менше у найбільшому виміру.
N2 – метастази в одному лімфатичному вузлі на стороні ураження до 6 см у найбільшому вимірі або метастази в лимфатичних вузлах шиї з обох сторін, або з протилежної сторони.
N2а – метастази в одному лімфатичному вузлі на стороні ураження до 6 см у найбільшому виміру.
N2b – метастазы в нескольких лимфатических узлах на стороне поражения до 6 см у найбільшому вимірі.
N2с – метастази в лімфатичних вузлах з обох сторін або з протилежної сторони до 6 см у найбільшому вимірі.
N3 – метастаз в лімфатичному вузлі більше 6 см у найбільшому вимірі.
МХ – недостатньо даних для визначення віддалених метастазів
М0 – немає ознак віддалених метастазів
М1 – наявність віддалених метастазів.
GХ – ступінь диференціювання не може бути встановлена.
G1 – висока ступінь диференціювання.
G2 – середня ступінь диференціювання.
G3 – низька ступінь диференціювання.
G4 – недиференційовані пухлини.
Наявність або відсутність залишкової пухлини після лікування позначається символом R.
RХ – Наявність залишкової пухлини не визначається.
R0 – Залишкової пухлини немає.
R1 – мікроскопічна залишкова пухлина.
R2 – макроскопічна залишкова пухлина.
|
I стадія |
Т1 NО М0 |
IV А стадія |
Т1 N2 М0 |
|
II стадія |
Т2 NО М0 |
|
Т2 N2 М0 |
|
III стадія |
Т3 NО М0 |
|
Т3 N2 М0 |
|
|
Т1 N1 М0 |
|
Т4а N0 М0 |
|
|
Т2 N1 М0 |
|
Т4а N1 М0 |
|
|
Т3 N1 М0 |
|
Т4а N2 М0 |
|
|
|
IV В |
Т4 b будь-яка N М0 |
|
|
|
|
Будь-яка Т N3 М0 |
|
|
|
IV С |
Будь-яка Т будь-яка N М1 |
Для встановлення діагнозу пацієнту призначаються дослідження: непряма ларингоскопія, ендоскопія, біопсія з первинного осередка пухлини, КТ з контрастуванням.
При відсутності морфологічного підтвердження раку (негативний результат біопсії) іноді необхідна повторна біопсія в тому числі і мікроларингоскопія або ендоскопія гнучким ендоскопом для визначення меж пухлини та її детальної характеристики. В деяких випадках, при ендофітних пухлинах проводиться діагностична тіреотомія.
Ендоскопічне дослідження в різних спектрах світла можливо виконати у великих центрах або інститутах для візуалізації та, при можливості, проведення прицільної біопсії.
Обстеження (зовнішній огляд, пальпація) при раку гортані має значення при наявності метастазів на шиї та при зміні контурів гортані.
У занедбаних стадіях раку гортані клінічна картина ускладнюється симптомами його поширення за межі ураженої гортані із залученням до процесу щитовидної залози, язика, глотки, трахеї, лімфатичних вузлів шиї , межестіння, блукаючого, поворотного і підязикового нервів, а також метастазами в інших органах. Діагностика раку гортані при цьому не важка, але лікування вже є малоефективним.
Діагностика раку гортані передбачає мікроларингоскопічне взяття зразків тканини з ділянки первинної пухлини/ Біопсія первинного ураження гортані з гістологічним дослідженням матеріалу. Якщо матеріал поганої якості – повторна біопсія до отримання результатів належної якості.
Для подальшого планування лікування обов'язковою є оцінка загального стану за шкалою Карновського або ECOG.
Оцінка функціональної придатності для радикального лікування (паралельно з визначенням діагнозу та стадії захворювання) передбачає оцінку загального стану, толерантності до фізичних навантажень, наявність супутніх захворювань, клінічної та радіологічної стадії.
Потенційна придатність для радикального лікування.
Непридатність або стадія, коли радикальне лікування неможливо провести, – це наявність суттєвої супутньої патології, яка зумовлюєпротипоказання до радикального лікування
Оцінка ризику для оперативного втручання проводиться з огляду на післяопераційні ускладнення, серцево-судинні ускладнення, смертність.
Можливість проведення радикального лікування (променевої або хіміотерапії, в тому числі, поєднаної хіміопроменевої терапії) визначається медико-діагностичною комісією (мультидисціплінарною командою спеціалістів).
Ураження пухлиною наступних структур пов’язане з поганим прогнозом або функцією*, або класифікується як Т4b (наприклад, неоперабельність з неможливістю технічно отримати чистий край). Жоден з цих чинників не є абсолютним протипоказом до операції в окремих пацієнтів, у яких можна тотально видалити пухлину:
* В окремих випадках потрібно розглянути можливість хірургічного лікування.
Об’єм видалення пухлини гортані залежить від уражених навколишніх структур. Первинна пухлина розглядається як операбельна, якщо широке видалення проводиться згідно до прийнятих критеріїв адекватного видалення в залежності від регіону ураження.
З метою зменшення ризику виникнення локального рецидиву проводиться оцінка країв резекції в режимі реального часу при застосуванні заморожених зрізів або відтерміновано при дослідженні тканин, зафіксованих у формаліні. Позитивний край збільшує ризик локального відновлення хвороби та є показом для післяопераційної ад’ювантної терапії. Якщо підтверджено позитивний край, повторна хірургічна резекція і/або ад’ювантна терапія показана для окремих пацієнтів.
Досягнення адекватних широких країв резекції може передбачати резекцію суміжних структур ротової порожнини та гортаноглотки, таких, як основа язика і/або передня частина язика, нижня щелепа, гортань, частина шийного відділу стравоходу.
Адекватна резекція – це чисті краї резекції, з достатньою частиною чистої від пухлини тканини, щоб можна було одержати чисті заморожені зрізи та постійні краї (переважно 1,5-2,0 см видимої та нормальної при пальпації слизової). При раку голосового відділу гортані 1-2 мм вважаються адекватними краями резекції. Оцінку заморожених зрізів країв резекції проводять інтраопераційно, особливо, коли є сумнів у достатній чистоті лінії резекції. При трансоральній лазерній мікрохірургії застосовуються краї резекції 1,5-2,0 мм з метою максимального збереження нормальних тканин за умови повної резекції пухлини. Чистота країв резекції підтверджується інтраопераційно методом оцінки заморожених зрізів. Такі краї вважаються «близькими» та можуть бути неадекватними для пухлин окремих локалізацій, як передня (ротова) частина язика.
Деталі країв резекції повинні бути включені в протокол операції. Оцінка країв резекції проводиться на видаленому препараті або альтернативно з хірургічного ложа пухлини при відповідному маркуванні орієнтації.
Чисті краї – відстань, що складає 5 мм і більше від інвазивного краю пухлини до резекованого краю.
Близькі краї – відстань, що складає менше 5 мм від інвазивного краю пухлини до резекційного краю.
Позитивний край – це рак in situ або інвазивна карцинома на краю резекції.
Первинну пухлину необхідно маркувати, зберігаючи орієнтацію. Пер-винна пухлина повинна бути оцінена гістологічно за наступними критеріями: глибина інвазії, відстань від інвазивної частини пухлини для країв резекції, враховуючи периферичні та глибокі краї резекції. У гістологічному звіті по-винна бути представлена інформація про первинний препарат, щоб повністю врахувати відстані від інвазивної частини пухлини до периферичних та глибоких країв резекції. Якщо хірург провів додаткову резекцію краю, то повинна бути збережена геометрична орієнтація резекційної пухлини та додаткових країв із зазначенням гістологом нових кінцевих країв резекції та їх гістологічного статусу.
Дисекція шиї повинна бути проведена таким чином, щоб згодом ідентифікувати рівні лімфатичних вузлів, включених у зону дисекції.
Реконструкцію хірургічних дефектів необхідно проводити за конвенційною технікою на розсуд хірурга (реконструктивне закриття дефекту локальними/реґіонарними лоскутами, вільними тканинними лоскутами, розщепленим шкірним лоскутом або іншими трансплантатами). За можливості рекомендовано первинне ушивання рани, однак при цьому не можна нехтувати збереженням широких країв резекції вільних від пухлини.
Оперативне втручання на лицевому нерві та інших основних лицевих нервах під час видалення первинної пухлини чи лімфодисекції реґіонарних лімфатичних вузлів залежить від клінічної функції нерву до операції.
Якщо нерв функціонує, необхідно зберегти його структуру і функцію (головний стовбур і/або його гілки), навіть коли відомо, що неможливо досягти адекватних країв резекції.
Ад’ювантна післяопераційна променева терапія або хіміопроменеве лі-кування показане у випадку, коли є підозра на мікроскопічну або клінічно видиму резидуальну пухлину.
При безпосередньому ураженні нерву пухлиною і/або при наявності передопераційного парезу нерву хірург на свій розгляд може провести сегментарну резекцію нерву (інколи пластику трансплантацією стовбура нерву), якщо на протязі всієї решти операції буде впевнений у досягненні країв резекції вільних від пухлини.
Хірургічне лікування реґіонарних лімфатичних вузлів визначається ступенем поширення первинної пухлини при первинному стадіюванні. Пацієнтам, яким проводиться резекція первинної пухлини, показана дисекція шиї з іпсілатеральної сторони, оскільки ця ділянка має найбільший ризик виникнення метастазів.
При пухлинах, що часто мають білатеральне дренування лімфи (напр., надголосниковий відділ гортані, перед надгортанниковий простір), нерідко необхідно проводити лімфодисекцію шиї з обох сторін з розширенням дисекції відповідно до вище наведених рекомендацій. При розташуванні пухлини по серединній лінії або близько до неї необхідно проводити дисекцію шиї з обох сторін. Елективна лімфодисекція не рекомендується, якщо у післяопераційному періоді планується променева терапія.
Проведення елективної лімфодисекції шиї базується на оцінці ризику наявності окультного метастазу у відповідному лімфатичному басейні. При плоскоклітинних карциномах порожнини рота глибина інвазії пухлини є найкращим предиктором окультних метастазів і повинна застосовуватися при виборі об’єму дисекції. При пухлинах з глибиною інвазії більше 4 мм строго показана елективна дисекція, якщо потім не планується ПТ. При пухлинах з глибиною інвазії менше 2 мм елективна дисекція показана лише у окремих випадках. При пухлинах з глибиною інвазії 2-4 мм необхідна клінічна оцінка (яке буде подальше спостереження, клінічні підозри та інші фактори) доцільності проведення елективної дисекції. Елективні дисекції у загальному є селективними із збереженням всіх основних структур, окрім випадків інтраопераційних знахідок, що вимагають розширення дисекції.
Вибір типу дисекції (комплексна або селективна) визначається відповідно до клінічної стадії перед операцією, міркувань хірурга та базується на первинному стадіюванні:
|
N0 |
Селективна дисекція шиї |
|
|
при раку гортані – хоча б рівні II-IV та рівень VI за необхідності |
|
N1-N2a-c |
Селективна або комплексна дисекція шиї |
|
N3 |
Комплексна дисекція шиї |
Дисекція шиї VI рівня проводиться при пухлинах певних локалізацій (напр., гортань, гортаноглотка), якщо це необхідно для радикального видалення первинної пухлини або при наявності будь-яких клінічних ознак ураження ЛВ даного рівня. Елективна дисекція залежить від поширеності первинної пухлини та її локалізації. При раку підголосникового відділу гортані часто проводять елективну дисекцію VI рівня.
Біопсія сторожового лімфатичного вузла є альтернативним по відношенню до елективної дисекції шиї методом ідентифікації прихованих (окультних) метастазів шиї у пацієнтів із раннім раком гортані, якщо вона рутинно виконується у спеціалізованих центрах. Перевагою даної методики є кращий косметичний ефект. Пацієнтам із метастатичною хворобою у сторожовому лімфатичному вузлу показана лімфодисекція шиї, а без – спостереження.
Радикальна променева терапія показана пацієнтам з раком гортані з I, II або III стадією із задовільним загальним станом (за шкалою ECOG 0, 1).
В плані стратегії органозберігаючої терапії при плануванні променевого лікування по радикальній програмі на різних установках (лінійні прискорювачі, та інші променеві апарати) потрібно брати до уваги ступінь диференціювання первинної пухлини.
Як правило, це дистанційна променева терапія, яка зазвичай застосову-ється у вигляді 1 фракції на день (1,8 – 2 Гр на фракцію), 5 днів на тиждень, протягом 5 - 7 тижнів.
Пацієнтам з І або II стадією , які з медичної точки зору неоперабельні, але підходять для радикальної променевої терапії, пропонують режим CHART – безперервна гіперфракційована прискорена радіаційна терапія. Або конформальна променева терапія (3D-CRT) на лінійних прискорювачах.
Пацієнтам зі стадіями III, які можуть отримувати променеву терапію і хто не може перенести або не бажає хіміотерапію, слід запропонувати схему CHART.
Якщо CHART неможливо виконати, повинна бути запропонована фракціонована променева терапія в дозі 64-66 Гр за 32-33 фракції 6 ½ тижнів, або 55 Гр за 20 фракцій протягом 4 тижнів.
а) тяжкі інфекційні ускладнення (емпієма плеври, асбсцедування ателектазу тощо);
б) активна форма туберкульозу;
в) супутні захворювання в стадії декомпенсації;
г) анемія (гемоглобін нижче 100 г/л), лейкопенія (нижче 3,0х109/л), тромбоцитопенія (нижче 145х109/л)
д) стан пацієнта за шкалою Карновського 40 та менше;
е) психічні розлади за наявності психомоторного збудження, яке проявляється руховою активністю.
IMRT використовується для зменшення віддалених токсичних ефектів при раку ротоглотки, параназальних синусів та носоглотки завдяки зниженню дози опромінення на слинні залози, темпоральні ділянки, слухову (включаючи кохлеарний апарат) та зорову системи.
IMRT та франціонування
Техніка SIB-IMRT використовує диференційований «розподіл дози» (66-74 Гр при великих пухлинах; 50-60 Гр при субклінічній хворобі) для кожної фракції лікування протягом всього курсу опромінення. SIB переважно застосовується по конвекційній (5 фракцій на тиждень) та «пришвидшеній» (6 фракцій на тиждень) схемі. Техніка SEQ-IMRT передбачає застосування початкової (низькі дози) фази (1-5 тиждень) з наступним переходом на фазу високодозового прискореного режиму (6-7 тиждень) з використанням 2-3 окремих планів дозування; переважно застосовується при стандартному фракціонуванні та гіперфракціонуванні. У супутньому графіку прискореного режиму може застосовуватися план дозування «модифікований SEQ», що передбачає доставку дози до субклінічних мішеней 1 раз на день протягом 6 тижнів та окремий план дозу-вання для другої фракції на день протягом останніх 12 днів лікування.
Паліативна ПТ повинна розглядатися у випадку запущеного раку, коли методики, скеровані на виліковування, не підходять.
У пацієнтів, яким стандартна ПТ не підходить, також при значній метастатичній хворобі, паліативна ПТ призначається для полегшення чи попередження локореґіонарних симптомів, якщо при цьому токсичність від ПТ є допустимою. Режими паліативної ПТ підбираються індивідуально. Рекомендовані наступні режими ПТ:
Незважаючи на коротші курси лікування необхідно обережно оцінювати толерантність спинного мозку та нейронних структур до дози фракціонування.
Необхідно ретельно оцінювати стан пацієнта, толерантність до лікування, відповідь пухлини на лікування і/чи будь-яке системне прогресування. Іншу паліативну/симптоматичну терапію, що передбачає застосування анальгетиків, харчування, тарґетну терапію, хіміотерапію «відчаю» застосовувати за показаннями.
При термінальних стадіях захворювання пацієнтам можна застосовувати більш гіпофракційні схеми у зв’язку із дуже поганим прогнозом.
ХТ проводиться пацієнтам з III або IV стадією раку гортані і задовільним загальним станом здоров’я (за шкалою ECOG 0-1 або за Карновським 80-100 балів).
Первинна (неоад’ювантна) ХТ призначається перед променевою терапією проводиться 2-3 циклами. При хорошій відповіді на лікування повному або частковому регресу первинного осередку чи метастазів призначається променеве або оперативне лікування.
Післяопераційна (ад’ювантна) ХТ може проводитись пацієнтам з задовільним статусом (за шкалою ECOG 0 або 1) і T2-3 N0 M0 при раку гортані, коли границі резекції після гістологічного дослідження мають елементи злоякісної пухлини.
ХТ занедбаного раку гортані включає комбінацію препаратів платини, фторурацилу, таксанів, гемцитабіну, які застосовують з урахуванням їх токсичності, ефективності та зручності.
Пацієнтам, які не можуть переносити схеми з препаратами платини, можна запропонувати ХТ з одним препаратом.
Монотерапію з доцетакселем слід розглядати, якщо лікування підходить для пацієнтів з місцевопоширеним або метастатичним раком гортані, у яких розвився рецидив після попередньої хіміотерапії.
Паліативна ХТ проводиться у пацієнтів із задовільним станом (за шкалою ECOG 0 або 1)
|
№ |
Склад схеми ХТ |
Кратність введення |
|
|
|
Основні схеми |
|
1. |
Цисплатин |
100 мг/м2 в режимі гідратації в/в крапельно в 1-й день. |
|
2. |
Цисплатин Доцетаксел |
80 мг/м2 в режимі гідратації 1-й день. |
|
3. |
Цисплатин Паклітаксел |
80 мг/ м2 в режимі гідратації 1 день . |
|
|
|
Додаткові схеми |
|
`1. |
Карбоплатин Паклітаксел Фторурацил |
400 мг/ м 2 1 день. |
|
|
|
Паліативні схеми |
|
1. |
Цисплатин Фторурацил |
75-100 мг /м2 в режимі гідратації в 1-й день. |
|
2. |
Доцетаксел Цисплатин фторурацил |
75 мг /м2 в день 1-й. |
|
3. |
Паклітаксел Карбоплатин |
175/мг/м2 1-й день. |
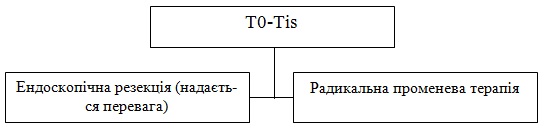
1. Ендоскопічна резекція МЛХ (надається перевага).
2. Радикальна ПТ в самостійному режимі:
Планований об’єм мішені (PTV)
Високий ризик: зони первинної пухлини та уражених реґіонарних лімфовузлів (включаючи можливе локальне субклінічне поширення первинної пухлини та рівні лімфатичних вузлів високого ризику)
Фракціонування:
Низький та середній ризик: зони підозрілі на субклінічне поширення 44-50 Гр (2,0 Гр/фракцію) до 54-63 Гр (1,6-1,8 Гр/фракцію).
3. Одночасна ХПТ
Планований об’єм мішені (PTV)
Високий ризик: звичайно 70 Гр (2,0 Гр/фракцію)
Низький та середній ризик: 44-50 Гр (2,0 Гр/фракцію) до 54-63 Гр (1,6-1,8 Гр/фракцію)
Рекомендується також ПТ з модульованою інтенсивністю (IMRT) або 3-D конформна ПТ (3-D CRT).
Примітки:
4. При проведенні хірургічного лікування виконуються відкриті резекції гортані + шийна дисекція за показаннями.
Після гістологічного дослідження матеріалу операції за наявності раку в межах резекції виконується повторна операція або радикальна променева терапія.
При екстракапсулярному поширені пухлини в лімфатичних вузлах – хіміопроменева терапія.
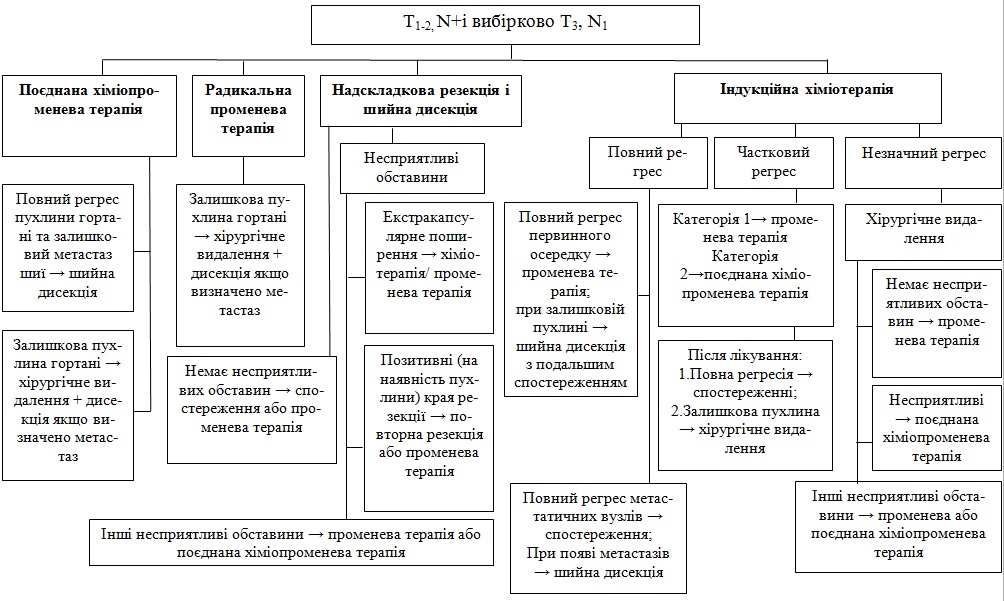
1. Поєднана ХПТ:
а) Повний регрес пухлини гортані – залишковий метастаз шиї – шийна дисекція.
б) Залишкова пухлина гортані – хірургічне видалення + дисекція якщо визначено метастаз.
2. Радикальна променева терапія
Залишкова пухлина гортані – хірургічне видалення + дисекція, якщо визначено метастаз.
3. Надскладкова резекція і шийна дисекція:
а) Немає несприятливих обставин – спостереження або променева терапія.
б) несприятливі обставини (екстракапсулярне поширення або/чи позитивні межі резекції) – повторна операція або проводиться поєднана хіміопроменева терапія.
г) Інші несприятливі обставини –ПТ або поєднана ХПТ.
4. Індукційна хіміотерапія.
Відповідь після індукційної хіміотерапії:
1. а) повний регрес первинного осередку – ПТ, при залишковій пухлині в лімфовузлах – шийна дисекція – подальше спостереження.
1. б) повний регрес метастатичних вузлів – спостереження після лікування, при появі метастазів – шийна дисекція, при відсутності метастазів – спостереження.
2. Частковий регрес первинного осередку – категорія 1 – ПТ; категорія 2- поєднана ХПТ.
Після лікування а) повна регресія – спостереження; б) залишкова пухлина – хірургічне видалення
3. Малий частковий регрес первинного осередку – хірургія (резекції гортані), при неможливості – ларингектомія
Після хірургії:
а) Немає несприятливих обставин –ПТ.
б) Несприятливі обставини (екстракапсулярне поширення або/чи позитивні межи резекції) – проводиться поєднана ХПТ.
в) Інші несприятливі обставини –ПТ або поєднана ХПТ.
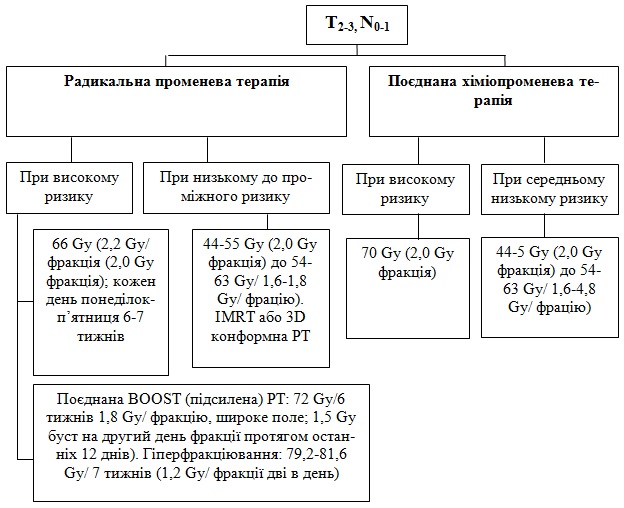
1. Радикальна променева терапія
При високому ризику: первинний осередок і включення лімфовузла (ве-лика вирогідність субклінічної інфільтації в пухлині і ризик наявності ланцюга лімфовузлів
Фракційовання:
а) 66 Гр (2,2 Гр/фракція) до 70 Гр (2,0 Гр/фракція); кожний день впродовж 6-7 тижнів.
б) BOOST (підсилена) ПТ: 72 Гр/ 6 тижнів. 1,8 Гр/фракцію, широке поле; 1,5 Гр (BOOST) на другий день фракції протягом останніх 12 днів.
в) Гіперфракціювання: 79,2 -81,6 Гр/ 7 тижнів (1,2 Гр на фракцію по дві на день).
г) При низькому до проміжного ризику: випадки з підозрою на субклінічне поширення 44-55 Гр (2,0 Гр/фракцію) до 54-63 Гр (1,6-1,8 Гр/фракцію).
д) Конформна ПТ або IMRT або 3D.
2. Поєднана ХПТ:
а) ХТ (цисплатин 100 мг/м2) проводиться кожний 3-й тиждень одночасно з ПТ (70 Гр), підведеною за 7 тижнів.
б) Високий ризик – типово гаматерапію підводять 70 Гр (2,0 Гр/фракцію).
в) Середній до низького ризику: 44-50 Гр (2,0 Гр/фракцію) до 54-63 Гр (1,6-4,8 Гр/фракцію).
3. Хірургічне лікування
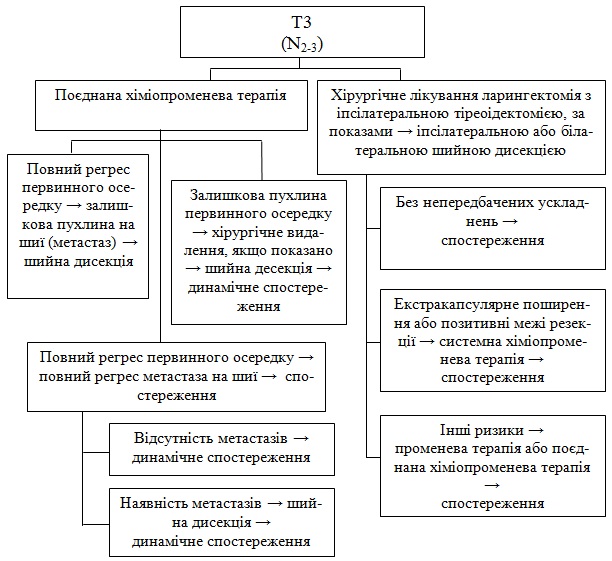
1. Поєднана системна ХТ/ПТ
а) При повному регресі первинного вогнища, якщо є залишковий вузол на шиї, – шийна дисекція. Якщо повний регрес вузла – спостереження, при негативному зростанні – подальше спостереження, при позитивному зростанні – шийна дисекція.
б) При резидуальному осередку – хірургічне лікування, за показаннями –шийна дисекція.
2. Ларингектомія іпсілатеральна тіреоідектомія з шийною дисекцією
а) При несприятливих умовах (екстракапсулярне поширення та/і позитивні межі резекції) – системна поєднана ХТ/ПТ; при рецидиві або залишковій пухлині – лікування, як при рецидивах або залишкових пухлинах.
б) При інших несприятливих обставинах – ПТ або поєднана ХПТ.
3. Індукційна хіміотерапія.
Відповідь після індукційної хіміотерапії:
1а) повний регрес первинного осередку – ПТ, при залишковій пухлині в лімфовузлах – шийна дисекція – подальше спостереження.
1б) повний регрес метастатичних вузлів – спостереження після лікування, при появі метастазів – шийна дисекція, при відсутності метастазів – спостереження.
2. Частковий регрес первинного осередку – категорія 1 – ПТ; категорія 2- поєднана ХПТ. Після лікування а) повна регресія – спостереження; б) залишкова пухлина – хірургічне видалення
3. Малий частковий регрес первинного осередку – хірургія (резекціі гортані), при неможливасті – ларингектомія
Після хірургії:
а) Немає несприятливих обставин –ПТ.
б) Несприятливі обставини (екстракапсулярне пширення або/чи позитивні межи резекції) – проводиться поєднана ХПТ.
в) Інші несприятливі обставини –ПТ або поєднана ХПТ
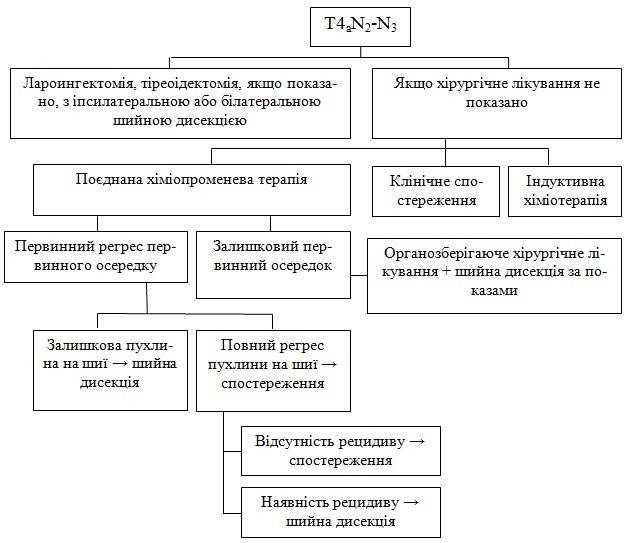
Повний регрес первинного осередку
Залишковий первинний осередок
При можливості виконання – оперативне втручання (ларингектомія + шийна дисекція якщо показано).
Якщо після лікування поєднаною ХПТ є рецидив або залишкова пухлина рекомендується або клінічне спостереження, або індуктивна хіміотерапія.
ПТ після хірургії
Інтервал після хірургії - менше або 6 тижнів:
Високий ризик – позитивні межі резекції, 60-66 Гр (2,0/фракцію), щоденно впродовж 6-6,5 тижнів.
Низький ризик – 44-50 Гр на фракцію-до 54-63 Гр(1,6-1,8 Гр на фракцію.
Післяхірургічна ХПТ
Поєднана ХПТ з одним агентом (Цисплатин 100 мг/м2 кожних 3 тижні).
Також рекомендується ПТ: 3-D або IMRT
1. Радикальна ПТ в самостійному режимі:
Високий ризик: зони первинної пухлини та уражених реґіонарних лімфовузлів (включаючи можливе локальне субклінічне поширення первинної пухлини та рівні лімфатичних вузлів високого ризику)
Фракціонування:
Низький та середній ризик: зони підозрілі на субклінічне поширення 44-50 Гр (2,0 Гр/фракцію) до 54-63 Гр (1,6-1,8 Гр/фракцію).
2. Одночасна ХПТ
Планований об’єм мішені (PTV)
Високий ризик: звичайно 70 Гр (2,0 Гр/фракцію)
Низький та середній ризик: 44-50 Гр (2,0 Гр/фракцію) до 54-63 Гр (1,6-1,8 Гр/фракцію)
Рекомендується також ПТ з модульованою інтенсивністю (IMRT) або 3-D конформна ПТ (3-D CRT).
Примітки:
5. Для T1-2, N0 може застосовуватися пришвидшене фракціонування.
6. При дозі ˃70 Гр для зменшення токсичності фракціонування повинно бути дещо змінене (напр., <2 Гр/фракцію хоча б протягом деякого часу лікування). Можна додати 2-3 дози в залежності від клінічної ситуації.
7. Пропонується 44-50 Гр на 3-D конформній ПТ з наступним планування IMRT або 54-63 Гр на IMRT (залежно від дози на фракцію).
8. При одночасній ХПТ найчастіше застосовується фракціонування 2,0 Гр за фракцію до сумарної дози 70 Гр за 7 тижнів з введенням цисплатину 100 мг/м2 кожні 3 тижні; проводиться 2-3 цикли хіміотерапії в залежності від схеми фракціонування променевої терапії.
3. Післяопераційна ПТ
Рекомендований інтервал між операцією та післяопераційною ПТ складає ≤ 6 тижнів.
Планований об’єм мішені (PTV)
Високий ризик: несприятливі фактори, такі, як позитивні краї – 60-66 Гр (2,0 Гр/фракцію); щоденно з понеділка до п’ятниці протягом 6-6,5 тижнів.
Низький та середній ризик: зони, підозрілі на субклінічне поширення, 44-50 Гр (2 Гр/фракцію) до 54-63 Гр (1,6-1,8 Гр/фракцію).
4. Післяопераційна ХПТ
Рекомендується супутнє одноразове введення цисплатину в дозі 100 мг/м2 кожні 3 тижні.
Рекомендується також ПТ з модульованою інтенсивністю (IMRT) або 3-D конформна ПТ (3-D CRT).
Ендоскопічне видалення (надається перевага) або радикальний курс ПТ.
Т1-Т2 або вибірково Т3 пацієнти, які підлягають органозберігаючій операції або (консервативній) ХТ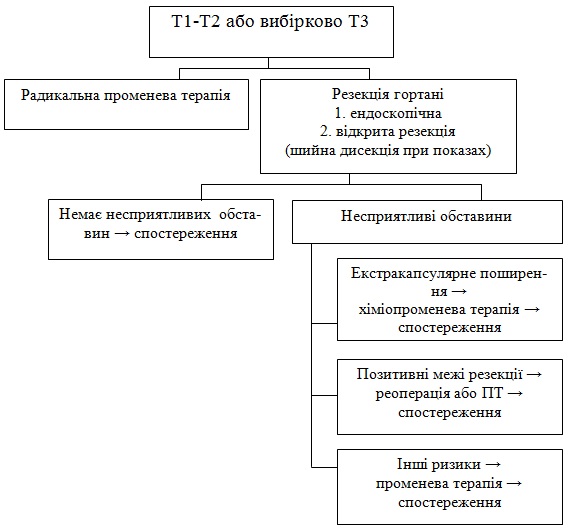
Радикальна променева терапія.
Резекція гортані (ендоскопічна або відкрита якщо показано шийна дисекція: немає несприятливих обставин – спостереження. За наявності несприятливих обставин:
а) екстракапсулярне поширення – ХПТ та спостереження;
б) позитивні межі резекції – повторна операція або ПТ- спостереження;
в) інші ризики – ПТ та спостереження.
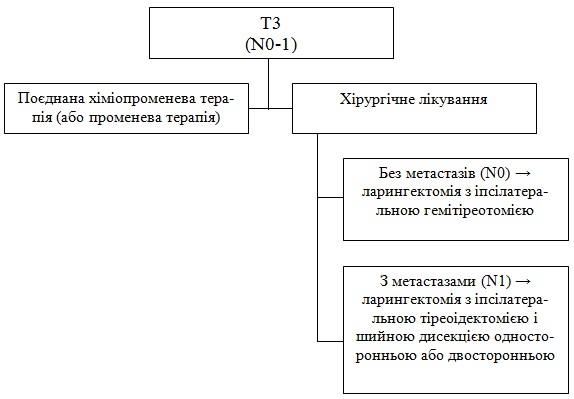
А) без (N0) метастазів- ларингектомія з гемітіреотомією іпсілатеральною.
Б) (N1) з метастазами- ларингектомія з іпсілатеральною тіреоідектомією і шийною дирекцією односторонньою або двосторонньою.
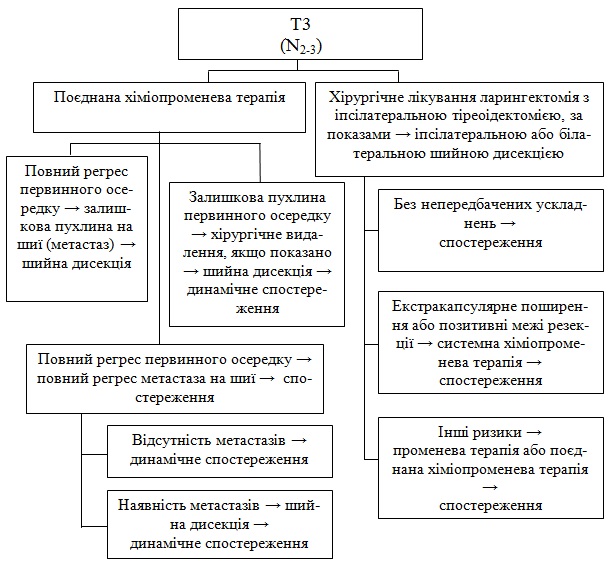
1. Поєднана ХПТ.
Після проведеного лікування первинного осередка:
а) Повний регрес осередка:
б) Залишкова пухлина (первиний осередок) - хірургічне видалення, якщо показано - шийна дисекція та динамічне спостереження.
2. Хірургічне лікування
Ларингектомія з іпсілатеральною тіреоідектомією, якщо показано, іпсілатерально/ або білатеральною шийною дисекцією:
а) Без непередбачених ускладнень – спостереження.
б) З ускладненнями:
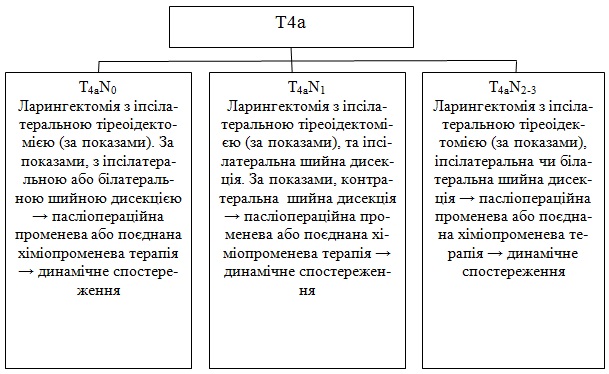
Ларингектомія з іпсілатеральною тіреоідектомією; якщо показано, іпсілатеральною або білатеральною шийною дисекцією, далі післяопераційна ПТ або поєднана ХПТ.
В подальшому динамічне спостереження.
Ларингектомія з іпсілатеральною тіреоідектомією; якщо показано, іпсілатерально чи контралатеральною дисекцією, далі - післяопераційна ПТ або поєднана ХПТ.
В подальшому динамічне спостереження.
Ларингектомія з іпсілатеральною тіреоідектомією; якщо показано, іпсілатерально чи контралатеральною дисекцією, далі - післяопераційна ПТ або поєднана ХПТ.
В подальшому динамічне спостереження.
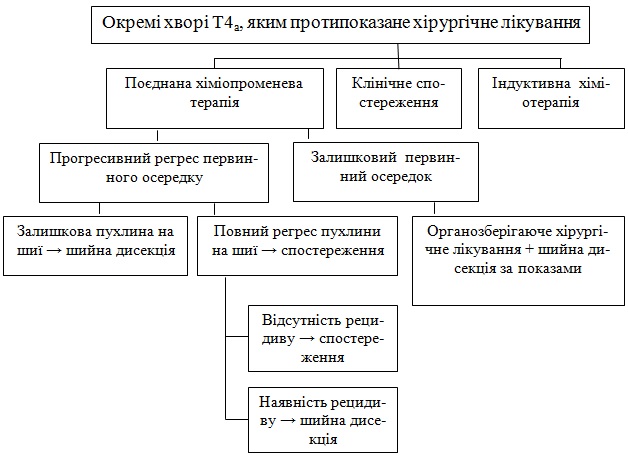
Поєднана ХПТ
Первинний осередок:
а) Повний регрес осередка: при залишковому метастазі на шиї- шийна дисекція- спостереження; при повному регресі метастаза на шиї – постлікувальна оцінка;
б) при відсутності метастазів на шиї –спостереження, при наявності метастазів – шийна дисекція та подальше спостереження.
Залишковий первинний осередок гортані:
а) Хірургічне видалення гортані + шийна дисекція, якщо показано – подальше спостереження.
б) Індукційна хіміотерапія.
При усіх стадіях розповсюдження виконується ларингектомія.
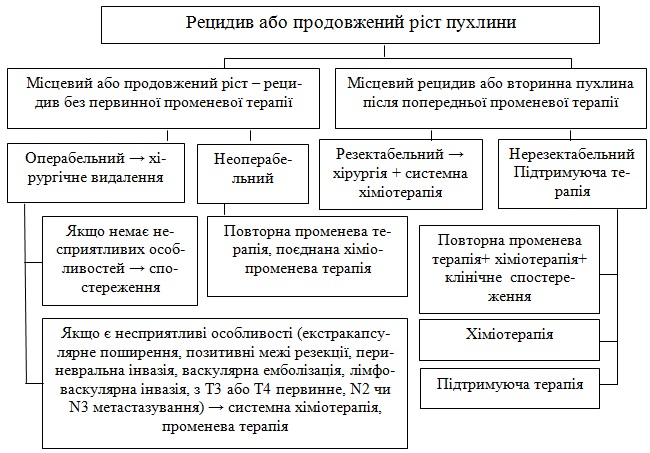
1. Якщо пацієнт операбельний – хірургічне видалення.
Якщо немає несприятивих особливостей – спостереження.
Якщо є екстракапсулярне поширення, позитивні межі резекції, перинев-ральна інвазия, васкулярна емболизація, лімфоваскулярна інвазія, рТ3 або з Т4 первинне, N2 чи N3 метастазування – системна ХТ, ПТ.
2. Якщо пацієнт неоперабельний – повторна променева терапія, поєднана ХПТ.
4.3.2. Місцевий рецидив або вторинна пухлина після попередньої ПТ
Тільки метастази:
Стандартна ХТ – препарат платини + фторурацил + цетуксимаб; комбінація ХТ, хірургія або ПТ, альтернативне лікування.
Метастази дистантні з регіонарним рецидивом:
Розглядається лікування що базується на ступені та симптомах захворювання.
Профілактика рецидиву захворювання здійснюється кількома способами:
а) реалізація принципів абластики і антибластики (при хірургічному втручанні) – максимальне видалення пухлинних клітин при первинному ліку-ванні за рахунок адекватного об’єму операції;
б) проведення ад’ювантної хіміотерапії.
в) своєчасне виявлення та адекватне лікування рецидивів і поодиноких метастазів.
Також необхідним є попередження та своєчасне виявлення злоякісних пухлин інших локалізацій у пацієнтів, які вилікувані від раку.
Паліативна ХТ проводиться у пацієнтів станом за ECOG – 0-1.
Метастази в головному мозку
Лікування церебральних метастазів включає кортикостероїди, опромінення всього мозку або стереотаксичну променеву терапію, хіміотерапію, таргетні препарати і хірургічну резекцію.
Компресія спинного мозку
Пацієнти з компресією спинного мозку повинні отримати лікування протягом 24-х годин. Застосовуються кортикостероїди, променева терапія, оперативне втручання там, де це необхідно. Якнайшвидше здійснюється направлення до фізіотерапевта для оцінки, лікування та реабілітації.
Метастази в кістки та патологічні переломи
Для пацієнтів з кістковими метастазами, які вимагають використання паліативних методів лікування та для яких стандартні знеболювальні препарати є неефективними, слід призначати однофракційну променеву терапію. При розвитку кісткових ускладнень застосувуються бісфосфонати.
Хронічний больовий синдром
Лікування пацієнтів здійснюється згідно медико-тезнологічних документів з надання медичної допомоги при хронічному больовому синдромі.
Інші симптоми, що свідчать про поширення злоякісного новоутворення в тому числі втрата ваги, втрата апетиту, втома, депресія і труднощі з ковтанням повинні лікуватися мультидисциплінарною командою згідно з відповідними медико-технологічними документами.
Нетрадиційні методи лікування
Як правило, спрямовані на полегшення симптомів шляхом емоційної та психологічної підтримки, і можуть використовуватися разом з іншими методами лікування раку. До них відносяться самодопомога через медитацію, релаксацію, контактна терапія (масаж), рефлексотерапія, ароматерапія, гомеопатія і акупунктура.
Ускладнення або реакції після спеціального лікування (хірургічного, променевої терапії, хіміотерапії) найчастіше можуть бути у вигляді розвитку дихальної недостатності втрата спілкування голосом у зв’язку з оперативним видаленням гортані. Тому реабілітація після лікування раку гортані включає фонопедію для формування стравохідного голосу та при неможливості та відновлення голосової функції голосовим протезуванням. Важливою є не тільки психосоціальна, але й трудова реабілітація.
Диспансеризація включає ретельне своєчасне обстеження пацієнтів, які закінчили лікування з приводу раку гортані, надання їм необхідної реабілітації та симптоматичної терапії, нагляд за пацієнтами з інкурабельними пухлинами, коригування симптоматичної терапії.
Періодичність диспансерного нагляду залежить від терміну з моменту закінчення спеціального лікування. Диспансеризація проводиться за місцем проведення спеціального лікування,
1. Обстеження, які виконуються протягом першого року після закінчення спеціального лікування.
1.1. Один раз на місяць перші 6 місяців:
а) Опитування та фізикальне обстеження;
б) Лабораторні дослідження крові з обов’язковим визначенням ШОЕ та біохімічних показників (ЛДГ, загальний білок, креатинин, сечовина, АЛТ, АСТ, рівень глюкози);
в) Рентгенографія органів грудної клітки;
г) УЗД шиї
д) КТ гортані з контрастуванням через місяць після лікування, при необхідності (за показами) в режимі ангіографії.
1.2. За наявності симптомів ураження:
а) КТ та МРТ головного мозку призначається при симптомах ураження ЦНС;
б) Ендоскопічне дослідження гортані;
в) Остеосцинтиграфія призначається при ознаках ураження кісток.
2. Обстеження, які виконуються протягом другого року після закінчення спеціального лікування.
2.1.Один раз на 4 місяці:
а) Опитування та фізикальне обстеження.
б) Лабораторні дослідження крові з обов’язковим визначенням ШОЕ та біохімічних показників (ЛДГ, загальний білок, креатинин, сечовина, АЛТ, АСТ, рівень глюкози);
в) Рентгенографія органівгрудної клітки:
г) ЕКГ;
2.2. За наявності симптомів ураження:
а) КТ та МРТ головного мозку призначається при симптомах ураження ЦНС;
б) Ендоскопія гортані при наявності симптомів ураження ФГДС шлун-ково-кишкового тракту;
в) ПЕТ призначається при ознаках ураження кісток.
3. Обстеження, які виконуються протягом третього – п’ятого років після закінчення спеціального лікування:
3.1. Один раз на 6 місяців.
а) Опитування та фізикальне обстеження.
б) Лабораторні дослідження крові з обов’язковим визначенням ШОЕ та біохімічних показників (ЛДГ, загальний білок, креатинин, сечовина, АЛТ, АСТ, рівень глюкози);
в) КТ органів грудної клітки;
г) ЕКГ;
3.2. За наявності симптомів ураження:
а) КТ та МРТ головного мозку призначається при симптомах ураження ЦНС;
б) Ендоскопічне дослідження гортані, ФЕГДС за наявності симптомів ураження шлунково-кишкового тракту;
в) ПЕТ призначається при ознаках ураження кісток.
Пацієнт перебуває на диспансерному обліку пожиттєво.
Інформація, опублікована на даному сайті, орієнтована на загальне ознайомлення та жодним чином не може бути використана в якості медичних, практичних або комерційних рекомендацій. У зв’язку з цим, Сайт «Школи доказової медицини» не несе жодної відповідальності за негативні наслідки, отримані через використання матеріалів, викладених на даному сайті. Документація з фармацевтичних продуктів не є рекламою та не призначена для того, щоб використовувати її замість консультації з кваліфікованими фахівцями в галузі медицини та інших галузях. Документація з фармацевтичних продуктів надається за вашою згодою відповідно до вимог ч.ч. 1, 2 ст. 15 Закону України «Про захист прав споживачів» від 12.05.1991 р. № 1023-XII. Якщо вам потрібна консультація з конкретного питання, пов’язаного зі здоров’ям, необхідно звернутися до фахівців- професіоналів.
Продовжуючи своє перебування на сайті, ви підтверджуєте свою згоду на дистанційне отримання інформації про лікарські та косметичні засоби (включаючи інформацію про рецептурні лікарські засоби) на підставі вимог ч.ч. 1, 2 ст. 15 Закону України «Про захист прав споживачів» від 12.05.1991 р. № 1023-XII.
Уся інформація, яка міститься на даному сайті, подана з освітньою метою виключно для медичних та фармацевтичних працівників і не замінює консультації лікаря.